Оксиды меди – это группа веществ, состоящих из атомов кислорода и меди. Выделяют несколько разновидностей оксида меди: I, II, III. Они отличаются физико-химическими свойствами. Соединения применяют в основном в стекольной промышленности, как красители, в качестве реагентов органической и неорганической химии, противогрибкового средства.
Содержание
- Что такое оксиды меди
- Виды (оксиды меди I, II и III), формулы
- Физические свойства, внешний вид
- Химические свойства, реакции
- Производство и получение оксидов меди I, II и III
- Применение (оксиды меди I, II и III)
- Опасность оксидов меди
- Где купить и сколько стоит
- Заключение
Что такое оксиды меди
Оксид меди представляет собой бинарное вещество, в котором кислород находится в степени окисления 2–, а свойства меди отличаются. Это амфотерный металл, способный вступать в превращения с кислотами и с щелочами за счёт различной валентности. Валентностью называют способность элемента удерживать возле себя другие атомы. Меди свойственна валентность I и II.
Виды (оксиды меди I, II и III), формулы
Оксид меди I – это закись меди, которая широко встречается в природе в минеральном виде. Формула меди оксида – Cu2O. Минерал куприт представлен кубическими кристаллами красного оттенка: от розового до ярко-алого. Иногда формируют слоистые, игольчатые образования. Проявляет алмазный блеск, твёрдость по шкале Мооса – 4. Месторождения расположены по всему миру: Франция, Россия (Урал), Намибия, Аризона.
Описывается оксид меди формулой CuO (II). В окружающей среде его находят в тенорите. Он распространён в форме громоздких неправильных чёрных масс. Характеризуется металлическим блеском и средней твёрдостью. Зоны раскопок сопряжены с сульфидными залежами, формируется в местах вулканической активности, был найден в лаве Везувия.
Оксид меди III – нестабильное вещество, которое удалось выделить только в ионных средах. Формула меди оксида III – Cu2O3.
Физические свойства, внешний вид

Внешний вид оксида меди II (порошок)
Свойства меди оксидов различны. Все они не растворяются в воде и органических растворителях: ароматических веществах, а также спиртах: метаноле, этаноле, в эфирах. Оксид меди I – твёрдый кристаллический порошок кирпично-красного цвета, реже тёмного, коричневатого.
Оксид меди II – мелкодисперсные чёрные кристаллы. Распадается при достижении отметки температурного режима в 1100 °C. Плотность 6,31 г/см3. Плавится при температуре 1447 °С, при нагревании до 2000 °С – закипает.
Свойства меди оксида III неизвестны.
Химические свойства, реакции
Оксиды меди реагируют со многими типами веществ. Так, оксид меди I взаимодействует с гидроксидом аммония:
Cu2O + 4(NH3 ∙ H2O) → 2[Cu(NH3)2]OH + 3H2O
Оксид меди реагирует с перманганатом калия:
Cu2O + KMnO4 + H2SO4 → 10CuSO4 + 2MnSO4 + K2SO4 + 13H2O
Оксид меди I реагирует с хлороводородом. При погружении в него оксида меди кислота даёт хлорид, выпадающий в осадок:
Cu2O + HCl → CuCl↓ + H2O
Активно реагируют с оксидом меди кислоты других неметаллов. Оксид меди I вступает в реакцию с азотистой кислотой:
Cu2O + 6HNO3 → 2Cu(NO3)2 + 2NO2↑ + 3H2O
Оксид меди I с угарным газом даёт окислительно-восстановительную реакцию:
Cu2O + CO → 2Cu↓ + CO2↑
По схожему механизму протекают реакции с другими газами:
Cu2O + H2 → 2Cu + H2O
Однако с кислородом оксид меди I проявляет восстанавливающие свойства:
2Cu2O + O2 → 4CuO
Оксид меди I при разогревании до 1800 °С разлагается, запускается реакция термолиза:
2Cu2O → 4Cu + O2
У оксида меди II слабо выражена амфотерность, это более сильный основный оксид. Особо выражено действие на оксид меди кислот. Вещество меди оксид реагирует с бромводородом:
CuO + HBr → 2CuBr2 + H2O
Оксид меди II взаимодействует с кислотными оксидами:
CuO + SO3 → CuSO4
Вещество меди оксид при смешивании с углеродом даёт металлическую медь и монооксид:
CuO + C → CO + Cu↓
Реакция взаимодействия оксида меди II с алюминием протекает с формированием глинозёма:
CuO + Al → Cu↓ + Al2O3
Производство и получение оксидов меди I, II и III
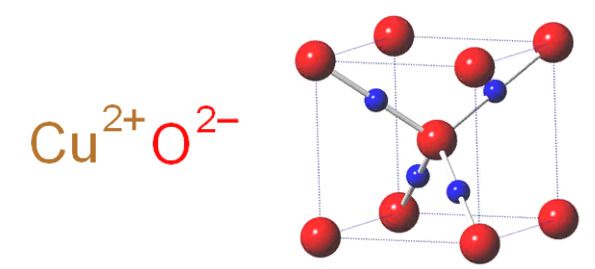
Химическая формула оксида меди II
В лабораторных условиях оксид меди получают разнообразными способами. Чаще всего применимо нагревание медной стружки в кислороде до 200 °С:
Cu + O2 → Cu2O
Для этого могут быть использованы реактивы йодида и гидроксида:
2CuI + KOH → Cu2O↓ + 2KI + H2O
В промышленности для синтеза оксида меди I пригодны высокотемпературные процессы (600 – 1300 °С):
4Cu + 2NO → 2Cu2O + N2↑
Для получения оксида меди I на заводе применяют прокаливание сульфида меди (I) при непрерывном вентилировании:
2Cu2S + 3O2 → 2Cu2O + 2SO2↑
Оксид меди II добывают из соответствующих гидроксидов:
2Cu(NO3)2 → CuO + 4NO2↑ + O2↑
Его можно получить и из природного сырья (малахит):
Cu2CO3(OH)2 → CuO + CO2 + H2O
Применение (оксиды меди I, II и III)
Основная сфера применения меди оксида – производство стекла. Благодаря наличию меди в составе вещество обладает выраженной окраской и способно передавать пигмент продукции.
Оксид меди I применяют для придания окраски керамическим и стеклянным изделиям. В качестве красителя его добавляют в глазури и водостойкие краски, которые наносят на суда. Оксид меди I обладает активностью пестицида, поэтому применение для прокрашивание им дна корабля защищает его от обрастания водорослями и, соответственно, разрушения.
Кроме того, применение меди оксида I распространяется на сферу сельского хозяйства. Вещество обладает противогрибковой активностью и работает как фунгицид. Оно нарушает целостность мембраны клеток патогенных микроорганизмов, дестабилизирует их, блокирует деление и рост мицелия. Применение оксида меди I эффективно для борьбы с такими микозами, как:
- мучнистая роса;
- пятнистости;
- серая и чёрная гниль;
- мумификация;
- млечный блеск;
- головня.
Применение оксида меди I способствует возвращению здорового вида растения, нормализации цветения и плодоношения. При соблюдении допустимых дозировок средство не наносит вреда растительным клеткам и не вредит урожаю. Обработку проводят в сухую безветренную погоду согласно инструкции.
Оксид меди II используется для окрашивания стекла в зелёный и синий цвета, производства витражей, медно-рубиновых стёкол. Другая сфера применения меди оксида II – химия. Это важный восстанавливающий реагент, необходимый для получения других соединений меди.
Опасность оксидов меди
Оксид меди I и оксид меди II относятся ко 2 классу опасности (высокоопасное вещество). При попадании на слизистую дыхательных путей вызывает сильное раздражение, ожоги, провоцирует кашель и перфорации. Неосторожное применение приводит к покраснениям кожи и появлению язв. При работе с оксидом меди I необходимо соблюдать меры осторожности, надевать защитную одежду и респиратор. Вещество крайне токсично для водной среды, поскольку убивает зоопланктон (рачков-дафний).
Где купить и сколько стоит
Оксиды меди можно приобрести в специализированных магазинах. 100 грамм оксида меди I – порядка 750 рублей. Стоимость оксида меди II – 1400 руб/100 г. Оптом вещества меди оксиды продаются заводами-производителями: от 40 руб/кг.
Заключение
Оксиды меди – это соединения меди с кислородом. Разновидности оксидов меди отличаются между собой, они не растворяются в воде, функционируют как окислители и восстановители. Основная сфера использования – выпуск цветных стёкол, а также садоводство и огородничество, где вещество используется как фунгицид, борющийся с грибковыми болезнями культурных растений. Оксиды меди I и II токсичны для человека и водных обитателей, обращаться с ними следует осторожно. Оксид меди III теоретически существует, но практически не был выделен.


